Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Sự khác nhau cơ bản giữa phi kim và kim loại SVIP
I. ỨNG DỤNG CỦA MỘT SỐ PHI KIM QUAN TRỌNG
Carbon, lưu huỳnh và chlorine là những phi kim có nhiều ứng dụng trong đời sống và sản xuất.
1. Carbon
- Trong tự nhiên, carbon đơn chất tồn tại ở dạng than chì (graphite), kim cương và carbon vô định hình (mồ hóng, than gỗ, than xương,...).
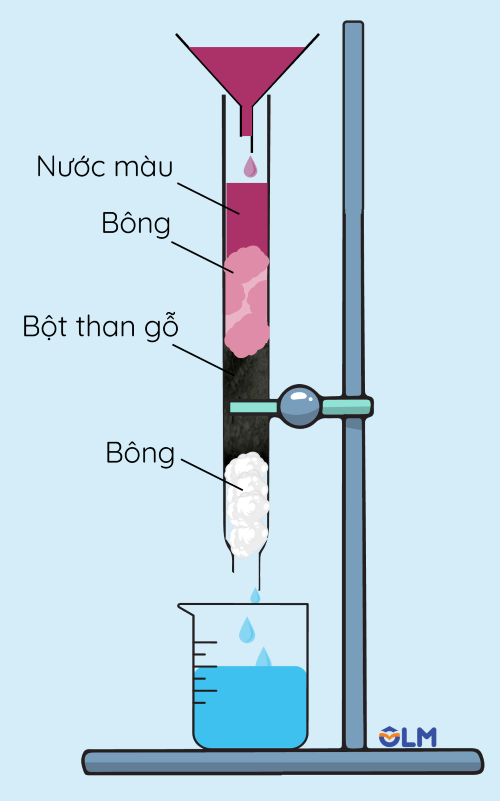
- Than gỗ, than xương,... có khả năng giữ lại các chất khí hoặc chất tan từ dung dịch trên bề mặt của chúng. Đặc tính này được gọi là tính hấp phụ.
Thí nghiệm tính hấp phụ của than gỗ
- Ứng dụng: than cốc là nguyên liệu cho quá trình luyện kim; than chì được dùng làm điện cực, ruột bút chì, chất bôi trơn,...; kim cương được dùng làm đồ trang sức, mũi khoan,...
2. Lưu huỳnh
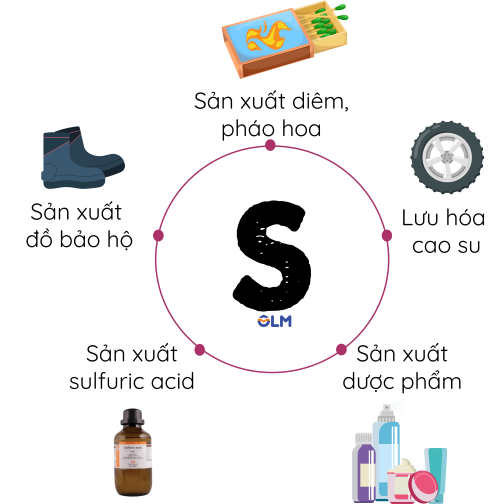
Ứng dụng của lưu huỳnh
3. Chlorine
Chlorine được dùng để khử trùng nước, sản xuất nước Javel, chất tẩy rửa, tẩy trắng vải, bột giấy và chế tạo chất dẻo.
Câu hỏi:
@202773688751@
II. SỰ KHÁC NHAU GIỮA PHI KIM VÀ KIM LOẠI
1. Sự khác nhau về tính chất vật lí
Hầu hết các nguyên tố phi kim không dẫn điện và có nhiệt độ nóng chảy, nhiệt độ sôi, khối lượng riêng nhỏ hơn so với kim loại.
a. Tính dẫn điện
- Hầu hết phi kim không dẫn điện, trong khi kim loại lại dẫn điện rất tốt.
- Silicon tinh khiết là chất bán dẫn.
- Than chì có thể dẫn điện nhưng kém hơn kim loại.
b. Nhiệt độ nóng chảy, nhiệt độ sôi
- Đa số phi kim có nhiệt độ nóng chảy và nhiệt độ sôi thấp hơn kim loại.
- Ở nhiệt độ thường, hầu kết kim loại tồn tại ở thể rắn (trừ thủy ngân) còn phi kim có thể tồn tại ở cả ba thể (rắn, lỏng, khí).
c. Khối lượng riêng
- Phi kim có khối lượng riêng nhỏ hơn kim loại.
Câu hỏi:
@202773721284@
2. Sự khác nhau về tính chất hóa học
- Kim loại thường nhường electron, phi kim thường nhận electron.
- Kim loại phản ứng với oxygen tạo oxide base, còn phi kim tạo oxide acid.
a. Phản ứng của kim loại với phi kim
Khi tham gia phản ứng hóa học, kim loại dễ mất electron để tạo thành ion dương, còn phi kim dễ nhận electron và trở thành ion âm.
Ví dụ 1:
\(Mg\rarr Mg^{2+}+2e\)
\(Br_{}+e\rarr Br^{-}\)
\(Mg+Br_2\rarr MgBr_2\)
Câu hỏi:
@202773764337@
b. Phản ứng của phi kim và kim loại với oxygen
- Kim loại tác dụng với oxygen tạo thành oxide base.
Ví dụ 2:
\(2Cu+O_2\overset{t^{o}}{\rarr}2CuO\)
- Phi kim tác dụng với oxygen tạo thành oxide acid.
Ví dụ 3:
\(C+O_2\overset{t^{o}}{\rarr}CO_2\)
Câu hỏi:
@202773770764@
Bạn có thể đăng câu hỏi về bài học này ở đây